Contre vents et marée, la recherche sur l’aluminium vaccinal avance
Voici en quelques mots l’état actuel des connaissances scientifiques sur le devenir de l’aluminium dans l’organisme après toute injection d’un vaccin aluminique, et sur les conséquences de la présence de cet adjuvant dans l’organisme.
Les nouveautés sont indiquées en italique. Elles font l’objet de trois publications (références en fin d’article) :
L’aluminium perdure de nombreux mois au site d’injection vaccinale
Simultanément, il migre dans l’organisme, principalement à l’intérieur des cellules immunitaires, et accède aux ganglions lymphatiques régionaux. Les cellules chargées de particules quittent ensuite le système lymphatique pour atteindre la circulation sanguine puis accéder à des organes distants tels que la rate, le foie et le cerveau.
Cette migration s’effectue plus ou moins rapidement et intensément selon 3 critères :
- Le site d’injection : la migration est plus rapide si l’injection est réalisée en sous-cutané plutôt qu’en intramusculaire (dans l’état actuel des connaissances, il n’existe pas d’éléments indiquant une différence de survenue d’effet indésirable selon que la vaccination est faite en intramusculaire ou en sous-cutané) ;
- La génétique : en cas d’altération des mécanismes de l’autophagie (processus de nettoyage de l’organisme qui permet d’éliminer les particules), la migration est plus rapide, induisant une bioaccumulation d’aluminium dans des sites sensibles en plus grandes quantité ;
- La concentration : une concentration modérée d’adjuvant aluminique forme des petits agrégats de particules qui migrent plus rapidement dans le cerveau qu’une concentration importante formant de gros agrégats.
La quantité d’aluminium s’accumule dans le cerveau…
Mais aussi dans les ganglions lymphatiques et la rate, organes du système immunitaire, en fonction des 3 critères ci-dessus. Cette accumulation est hautement contre-indiquée, compte-tenu de la (neuro)toxicité de l’aluminium. Elle pourrait être à l’origine non seulement des manifestations typiques associées à la myofasciite à macrophages mais aussi d’autres pathologies (scléroses en plaques post-vaccinales, encéphalomyélites aigues disséminées, certains cas d’autisme…), comme l’indiquent les travaux de plusieurs scientifiques (Pr Shaw – Canada, Dr Seneff – USA).
Les autorités sanitaires disposent de ces résultats.
>>> Pour soutenir financièrement la poursuite de ces recherches, cliquez ici <<<
Trois articles publiés en 2015 viennent détailler ces résultats :
Article 1 : Suivre le cheminement de l’aluminium vaccinal dans l’organisme animal
Le premier article que nous souhaitons évoquer est paru en juin 2015 dans BMC Medicine : « Des nanodiamants fluorescents comme marqueurs pertinents pour l’évaluation de la biodisposition des particules d’adjuvants aluminiques », par Housam Eidi et al.
L’équipe de l’hôpital Henri Mondor (Créteil) vient de mettre au point un traceur très prometteur permettant de suivre très précisément le cheminement de l’aluminium vaccinal dans l’organisme animal, y compris à des niveaux faibles et sur le long terme. Il s’agit du « complexe AluDia », qui combine des nanodiamants fluorescents et l’adjuvant aluminium.
Cette technologie de choix va pouvoir dorénavant être utilisée pour l’étude de la distribution, de la persistance et de la neurotoxicité à long-terme des adjuvants aluminiques, voire d’autres types de nanoparticules.
=> Lire l’article original : http://www.ncbi.nlm.nih.gov/pubmed/26082187
=> Lire quelques extraits en français
Article 2 : Analyser les troubles cognitifs chez les personnes atteintes de myofasciite à macrophages
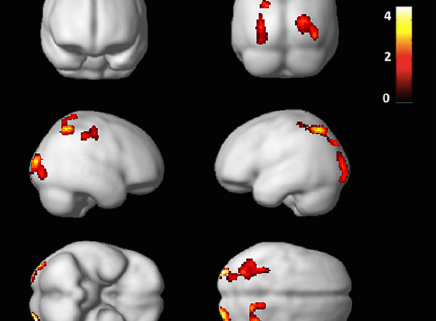
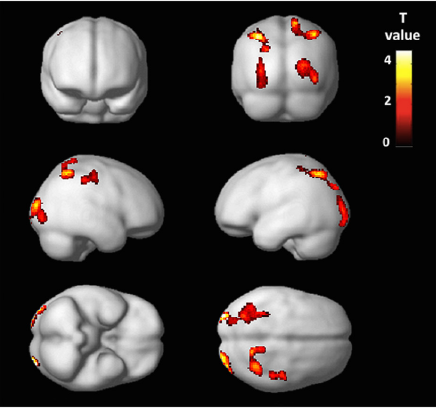
Le deuxième article est paru en juin 2015 dans la revue Plos One : « Corrélats neuropsychologiques de SPECT par perfusion cérébrale chez des patients atteints de myofasciite à macrophages », par Axel Van der Gucht et al.
Les patients atteints de myofasciite à macrophages (MFM), une pathologie neuromusculaire induite par les sels d’aluminium utilisés comme adjuvant vaccinal, souffrent d’arthromyalgies, de fatigue chronique et de déficits cognitifs. Cette étude vise à caractériser les atteintes cérébrales chez ces patients.
Une tomographie par émission de photon simple (SPECT) par perfusion cérébrale a été réalisée sur 76 patients consécutifs (âgés de 49 ± 10 ans) suivis au centre de référence des maladies neuromusculaires rares Garches-Necker-Mondor-Hendaye.
Cette étude a révélé des changements corticaux et sous-corticaux identiques chez l’ensemble des patients, qui correspondent aux troubles cognitifs associés à la MFM décrits dans des études précédentes.
Ces résultats permettent de faire un lien entre les dysfonctionnements cognitifs observés chez les patients atteints de MFM et des atteintes cérébrales objectivées par la technique du SPECT.
=> Lire l’article original : http://www.ncbi.nlm.nih.gov/pubmed/26030650
=> Lire quelques extraits en français
Article 3 : Déterminer le fonctionnement de l’adjuvant aluminium après injection
Le troisième article est paru en novembre 2015 dans la revue Journal of Inorganic Biochemistry : « Translocation systémique retardée d’adjuvant à base d’aluminium chez des souris CD1 après injection intramusculaire », par Guillemette Crépeaux et al.
Jusqu’à présent, les études sur le devenir des sels d’aluminium après injection étaient menées sur les souris de laboratoires « C57BL/6 », qui ont l’avantage d’être issues d’une lignée stable et à reproduction facile. Elles servent habituellement de modèles physiologiques ou pathologiques pour des expériences in vivo.
Dans cette étude, un vaccin aluminique et de l’aluminium marqué avec des nanodiamants fluorescents récemment mis au point (AluDia) ont été utilisés sur des souris « CD1 » (souris non-consanguines avec donc une variabilité génétique) pour évaluer :
– la durée de persistance au site de l’injection,
– la translocation de l’aluminium du site de l’injection vers les organes lymphoïdes
– le comportement de ces souris suite à l’injection intramusculaire de l’aluminium (400 μg d’Al/kg).
Les résultats ont montré pour la première fois une translocation systémique des particules de l’adjuvant étonnamment retardée. Le granulome induit par l’injection d’aluminium est resté dans le muscle pendant une très longue période malgré une rétraction progressive. De manière concomitante, une translocation sensiblement retardée de l’aluminium dans les ganglions lymphatiques et la rate a été observée. Contrairement aux souris C57BL/6J, aucune hausse du niveau d’aluminium dans le cerveau ni de changement comportemental n’ont été observés.
Sur la base de précédents rapports présentant les effets neurotoxiques de l’aluminium chez les souris CD1, une expérience complémentaire a été menée, montrant une translocation précoce au jour 45 de l’aluminium injecté par voie sous-cutanée.
Cette étude démontre ainsi l’importance de la souche de souris, de la voie d’administration et des doses pour les études futures se concentrant sur les effets toxiques potentiels des adjuvants à base d’aluminium.
=> Lire l’article original : http://www.ncbi.nlm.nih.gov/pubmed/26384437



Bonjour,
Pour bien comprendre la problématique tu site d’injection, quand vous dites que « la migration est plus rapide si l’injection est réalisée en sous-cutané plutôt qu’en intramusculaire », est-ce que cela veut donc dire qu’il est préférable de faire l’injection en intramusculaire ?
Merci
En l’état actuel des connaissances, il semblerait que oui…